Spina bifida — порок развития позвоночника (спинальный дизрафизм или рахишиз), часто сочетающийся с грыжей оболочек (менингоцеле или менингомиелоцеле), выбухающих через дефект кости. Она также часто сочетается с дисплазией спинного мозга (миеложисплазией), когда нервная трубка формируется не из собственно нервной пластинки, спинной мозг остается в примитивной форме (миелошизис). Этот факт вызывает различную степень пороков развития нервной трубки. Центральная нервная система возникает на 3-й неделе эмбрионального развития. Нервную пластинку можно выявить в дорсальной части средней линии эмбриона на инициальной стадии, в течение нескольких дней она выпячивается, формируя нейрональные складки. Нейрональные складки углубляются и перемещаются к средней линии, образуя нейрональный желобок.
В большинстве случаев spina bifida возникают в результате нарушения закрытия концов нервной трубки или их повторного открытия. У человека нервная трубка формируется из эктодермы, ее замыкание происходит на 21-28-й день после зачатия. При нарушении процессов формирования нервной трубки в зависимости от места появления дефекта образуется либо анэнцефалия, либо spina bifida. Возникновение spina bifida обусловлено как наследственными факторами, так и воздействием факторов внешней среды. Среди наследственных особенностей можно выделить половые и этнические различия, повышенную степень конкордантности у монозиготных близнецов, мутации генов и хромосомные нарушения.
Необходимо учитывать факт рождения детей с spina bifida в анамнезе и наследственном анамнезе. Повышать риск появления spina bifida могут лекарственные средства, нарушающие обмен фолатов (триметоприм, сульфасалазин, карбамазепин, фенитоин, вальпроевая кислота и другие противосудорожные средства и т. д.), злоупотребление алкоголем, метанол. К приобретенным факторам, способным приводить к возникновению ДНТ, относят сахарный диабет, гипертермию, курение и т. д. Определенную роль в развитии патологии могут, кроме того, играть такие факторы, как место проживания, время года, в которое произошло зачатие, возраст матери, социально-экономические условия, а также алиментарный фактор.
Патогенез спинального дисрафизма точно не установлен. Существует две теории: одна — это нарушение закрытия нервной трубки, которая выдвинута Рекленгаузеном в 1886 году. Другая патогенетическая теория — гидродинамическая, выдвинутая Моргани в 1761 году. Кроме двух указанных теорий существует теория чрезмерно ускоренного роста или остановки роста как причина дизрафии нервной трубки.
Частота spina bifida колеблется от 1 до 2 на 1000 новорожденных. Частота повторных родов с этим пороком от 6 % до 8 %, что говорит о генетическом факторе развития заболевания. Более высокая частота данной патологии у детей, родившихся от более пожилых матерей. Однако, несмотря на эти данные, 95 % новорожденных со spina bifida рождаются у родителей, у которых не было spina bifida. Другие факторы, такие как краснуха, грипп, тератогенные вещества — являются предрасполагающими.
ДНТ были описаны еще древними египтянами, а в 1641 г Tulp N. Впервые изобразил spina bifida. Алиментарный фактор одним из первых был признан фактором риска развития spina bifida. Stein и соавт. отметили высокую частоту spina bifida у 18-летних юношей, поступающих на военную службу, которые были рождены во время голода в конце Второй мировой войны. В дальнейшем Hibbard и Smithells показали, что женщины, родившие детей с дефектами нервной трубки, во время беременности испытывали дефицит витаминов. По их наблюдениям, в результате приема мультивитаминных комплексов частота рецидивов этой патологии в последующие беременности резко сократилась.
Steegers-Theunissen R.P. и соавт. впервые предположили наличие связи между нарушением фолатзависимых процессов обмена гомоцистеина и развитием дефекта нервной трубки (коэффициент несогласия – 6,8; 95 % доверительный интервал). В дальнейшем они показали, что риск формирования spina bifida возрастает при повышении концентрации гомоцистеина в крови, а прием фолиевой кислоты в свою очередь снижает содержание гомоцистеина в плазме крови беременных. Концентрация гомоцистеина в амниотической жидкости у новорожденных, родившихся с дефектами нервной трубки, была выше, чем у таковых контрольной группы. При изучении обмена метионина в экстраэмбриональной и амниотической жидкостях было показано, что концентрация общего гомоцистеина в эмбриональной жидкости значительно ниже, чем в плазме крови матери, а концентрация метионина в четыре раза выше в экстраэмбриональной целомической жидкости и в два раза – в амниотической жидкости по сравнению с плазмой крови матери.
В Дании van der Put N.M. и соавт. выявили повышенную частоту полиморфизма С677Т гена фермента метилентетрагидрофолат редуктазы (МTHFR) у членов семей, в которых имелись дети с дефектами нервной трубки. Мутация гена выявлена у 16 % матерей, 10 % отцов и 13 % новорожденных со spina bifida по сравнению с 5 % в контрольной группе. Подобные результаты были получены и в других странах. В данном исследовании показано, что риск развития spina bifida повышается в семь раз при сочетании гомозиготной мутации у матери и у плода. Это доказывает влияние нарушений обмена гомоцистеина у плода на развитие дефектов нервной трубки.
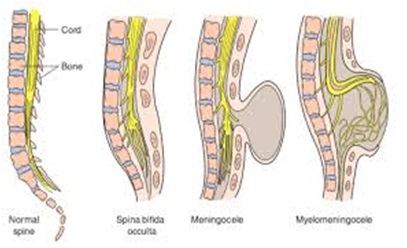
Выделяют три формы spina bifida:
Spina bifida occulta. Часто эта форма называется «скрытая spina bifida», так как при этом спинной мозг и нервные корешки в норме, а также отсутствует дефект в области спины. Данная форма характеризуется лишь небольшим дефектом или щелью в позвонках, которые формируют позвоночный столб. Зачастую эта форма патологии настолько умеренно выражена, что не вызывает каких-либо беспокойств. При этом такте больные даже не знают о наличии у себя этого порока развития и узнают об этом лишь после рентгенографии. Чаще всего эта форма spina bifida возникает в пояснично-крестцовом отделе позвоночника. У 1 из 1000 больных данной формой патологии могут отмечаться проблемы с функцией мочевого пузыря или кишечника, боли в спине, слабость мышц ног и сколиоз.
Менингоцеле. Возникает когда кости позвоночника не закрывают полностью спинной мозг. При этом мозговые оболочки через имеющейся дефект выпячиваются в виде мешочка, содержащего жидкость. Этот мешочек состоит из трех слоев: твердой мозговой оболочки, паутинной оболочки и мягкой мозговой оболочки. В большинстве случае спинной мозг и нервные корешки нормальны либо с умеренным дефектом. Очень часто «мешочек» мозговых оболочек покрыт кожей. Это состояние может потребовать хирургическое вмешательство.
Миеломенингоцеле (spina bifida cystica) . Эта форма составляет около 75 % всех форм spina bifida. Это наиболее тяжелая форма, при этом через дефект позвоночника выходит часть спинного мозга (так называемая мозговая грыжа). В некоторых случаях «мешочек» со спинным мозгом может быть покрыт кожей, в других случаях наружу могут выходить сама ткань мозга и нервные корешки. Степень неврологических нарушений напрямую связана с локализацией и тяжестью дефекта спинного мозга. При вовлечении в процесс конечного отдела спинного мозга, могут отмечаться нарушения только мочевого пузыря и кишечника. Более тяжелые дефекты могут проявляться в виде параличей ног вместе с нарушением функции мочевого пузыря и кишечника.
Первый порок не сочетается с грыжами оболочек и может никак не проявляться до взрослого возраста. Менингоцеле содержит только ликвор, а нервные элементы отсутствуют. При миеломенингоцеле есть и ликвор и нервная ткань. Миелоцистоцеле — локальное расширение центрального канала с выбуханием задней стенки спинного мозга. Миелоцеле — выбухание спинного мозга в мешок через дефект кости. В редких случаях нервная трубка отсутствует и спинной мозг остается на уровне примитивной формы, напоминающей нервную пластинку (spina bifida aperta).
Спина бифида оккульта чаще взникает в пояснично-кресцовом отделе. Костный дефект можно пропальпировать. Спина бифида оккульта часто сочетается с диастематомиэлией, фиксированным спинным мозгом, липоменингоцеле, неуроэнтерической кистой с дермальными или эпидермальными опухолями. Эти проявления обычно не дают клинических симптомов до тех пор, пока ребенок не начинает ходить и не начинает осуществлять контроль за актами дефекации и мочеиспускания. Могут быть выявлены ненормальности кожи на спине в 75% больных со скрытым спинальным дисрафизмом. Могут наблюдаться локальное оволосение, капиллярные гемангиомы, покрытая ямочками кожа.
Часто отмечается истечение ликвора. Около 80% миеломенингоцеле возникает в поясничном и пояснично-сакральном районе. Около половины менингоцеле бессимптомны, а частота сочетания с гидроцефалией составляет около 25%, тогда как при миеломенингоцеле частота гидроцефалии составляет 70-80%. Гидроцефалия может развиться и после устранения миеломенингоцеле. В развитии послеоперационной гидроцефалии могут приводить следующие механизмы: дефект зоны абсорбции ликвора при удалении мешка, окклюзия менигеальных пространст после менингита.
Окллюзия ликворного оттока из 4-го желудочка обусловленное ущемлением продолговатого мозга в большом затылочном отверстии при мальформации Арнольда-Чиари. У большинства детей с миеломенингоцеле имеются неврологические симптомы, чаще моторная слабость в нижних конечностях, чувствительные расстройства. Когда повреждение расположено выше сегмента L3 возникает полная параплегияи и пациент постоянно остается неподвижным. Если повреждение ниже сегмента L4 параплегия отсуствует, но есть симптомы недержания мочи различной степени. Уровень двигательных расстройств определяется наличием произвольных движений в бедре, колене, стопе. Чувствительные расстройства проверяются уколами в зоне выпадения к зоне нормальной чувствительности.
Новорожденные со spina bifida нуждаются в лечении, направленном на восстановление целостности, чтобы предотвратить в последующем травму или инфицирование. Нейрохирург при этом помещает ткани обратно в спинномозговой канал и закрывает имеющийся дефект. При необходимости закрытия большого участка дефекта, может потребоваться помощь и пластического хирурга. Обычно такие операции являются неотложными и проводятся через несколько часов после рождения ребенка.
Примерно у 80 – 90 % детей со spina bifida развивается и гидроцефалия. Это заболевание, характеризующееся избыточным количеством цереброспинальной жидкости в желудочковой системе головного мозга и/или в субарахноидальных пространствах. Большинству таких детей требуется шунтирующая операция. Принцип операции в следующем – «избыточный» ликвор с помощью систем трубок и клапана выводят в естественные полости организма человека (вентрикуло-перитонеальное шунтирование – в брюшную полость, вентрикуло-атриальное – в правое предсердие и т.д.). после операции шунт у больного остается на всю жизнь. Правда, все же, несколько раз его нужно будет заменить.
Несмотря на успехи в ранней диагностике дефектов развития нервной трубки, благодаря внедрению в практику биохимических методик (исследование содержания α-фетопротеина и ацетилхолинестеразы в сыворотке крови матери и околоплодных водах), методов интраскопии плода (ультразвуковой, ядерно-магнитный) основное значение в снижении частоты этой аномалии принадлежит предупредительным мероприятиям. Учитывая, что причины возникновения дефектов развития нервной трубки многофакторные и эти факторы известны, обоснованно формирование групп риска беременных, у которых вероятность рождения ребенка с дефектом наиболее высока. Поэтому во всем мире признано, что при планировании беременности родителям необходимо обследоваться у врача-генетика, а будущей матери у гинеколога, чтобы предпринять меры по профилактике уродств развития нервной трубки, отнести беременных к различным группам риска и с различной настороженностью контролировать течение беременности.
Оптимальный алгоритм пренатального обследования для снижения частоты дефектов развития нервной трубки предполагает следующее.
1. В период планирования беременности — консультации врача-генетика, терапевта, акушера-гинеколога, при необходимости уролога. Выделение групп беременных с высоким и низким риском рождения ребенка с дефектом развития нервной трубки.
2. Пренатальная диагностика и объем обследования беременных отличаются в различных группах риска.
В группах низкого риска проводятся:
— ежемесячные консультации (осмотры) акушером;
— во втором триместре беременности анализ крови беременной на содержание α-фетопротеина и ацетилхолинестеразы (при повышенных уровнях — повторный анализ их содержания в околоплодных водах и ультразвуковое обследование плода). Если наличие дефекта нервной трубки подтверждается, ставится вопрос о прерывании беременности;
— в третьем триместре беременности — ультразвуковое исследование и подготовка к родам.
В группах высокого риска проводятся:
— ежемесячный осмотр акушером;
— во втором триместре беременности обязательный многократный контроль содержания α-фетопротеина и ацетилхолинестеразы в сыворотке крови и околоплодных водах, многократное ультразвуковое исследование плода с целью обнаружения возможных врожденных уродств развития плода, в сложных ситуациях используют магнитно-резонансное обследование.
Подтверждение дефекта развития нервной трубки — обычно основание для прерывания беременности, но современные методы пренатальной диагностики не являются абсолютными. Они чаще диагностируют сам факт наличия дефекта, однако не всегда можно уточнить степень выраженности его. В то же время, степень вовлечения в патологический процесс нервных структур считается определяющей для прогноза. При менингоцеле и своевременной хирургической помощи ребенок полноценно развивается, а в будущем становится нормальным трудоспособным человеком. При менингомиелоцеле даже хирургическая помощь не обеспечивает высокого качества жизни, ребенок будет инвалидом, нередко тяжелым. Поэтому обнаружение у плода дефекта развития нервной трубки — всегда веское основание для прерывания беременности.
Значительно сложнее ситуация в семьях, где беременность долгожданна, а перспектива новой беременности маловероятна. Если выраженность дефекта уточнить не удается, используют дополнительные методы диагностики: ядерно-магнитную резонансную томографию (МРТ), но и она не всегда позволяет ответить на поставленные вопросы. Тогда врачи совместно с родителями, объясняя все обстоятельства и возможные исходы, решают судьбу плода.
Если у ребенка нет противопоказаний (тяжелые сопутствующие уродства развития других органов или необратимые неврологические расстройства), при spina bifida производят операцию, которая заключается в выделении грыжевого мешка и его ножки из окружающих тканей, вскрытии этого мешка и осмотре его содержимого. При наличии в полости грыжевого мешка корешков спинного мозга их осторожно выделяют, погружают в спинномозговой канал, мешок иссекают и остатки его сшивают над спинным мозгом. Щель в дужках закрывают мышечно-фасциальным лоскутом. Операция избавляет больных от грыжевого выпячивания, но менее благоприятна в смысле обратного развития неврологических нарушений, что является следствием необратимых дегенеративных изменений спинного мозга и его корешков. Если у ребенка со spina bifida имеется параплегия (то есть паралич обеих ног), то он будет вынужден пользоваться инвалидным креслом. При наличии движений в области бедер у ребенка имеются хорошие шансы, он может передвигаться с помощью особых подпорок. К счастью, больные со spina bifida могут вести активный образ жизни при соответствующем уходе за ними.
Последние 10 лет гинекологи могут предупреждать пороки развития нервной трубки плода. Это можно сделать, если женщина принимает конкретную дозу (400 микрограмм в день) фолиевой кислоты при планировании беременности и вплоть до истечения первого триместра беременности, поскольку нервная трубка плода закладывается именно в этот период. В странах Европейского союза этот вопрос уже становится социально значимым, система здравоохранения вводит правила обязательного приема фолиевой кислоты. Речь идет о таких странах как Франция, Великобритания, Ирландия, Норвегия, Финляндия, Испания, Италия. Существует ряд исследований, доказавших, что ежедневный прием 400 микрограмм фолиевой кислоты предупреждает развитие пороков нервной трубки плода. В 2005 году Министерство здравоохранения Италии утвердило закон, в соответствии с которым фолиевая кислота в дозировке 400 микрограмм включена в перечень лекарственных средств, обязательно выдаваемых по медицинской страховке всем планирующим беременность женщинам. В соответствии с этим законом, по заказу Министерства Италии, компания Италфармако занимается производством препарата Фолибер. Министерство здравоохранения Италии, в рамках национальной программы, ставит своей целью на протяжении 5 лет снизить частоту развития spina bifida на 60% путем приема препарата Фолибер.

 English
English Русский
Русский Հայերեն
Հայերեն